Indépendamment de leur origine biologique, la plupart des protéines sont composées de plusieurs domaines élémentaires reliés entre eux par des connecteurs protéiques. Ces domaines sont soit des unités fonctionnellement indépendantes, soit des parties de structures multidomaines plus larges, dont les fonctions sont liées à leur proximité spatiale. C’est le cas pour les enzymes impliquées dans la déconstruction des parois végétales. Afin d’interroger l’effet de la proximité et de la géométrie spatiale de ces domaines sur la catalyse, nous avons utilisé une approche originale qui consiste à souder entre eux deux domaines en utilisant deux petites protéines Jo et In ; la particularité est que Jo et In nous permettent de figer nos enzymes dans des conformations spatiales contrôlées et de tester leur activité sur des substrats insolubles.
Une autre approche a consisté à créer une plateforme protéique chimérique constituée de trois domaines, dont un permet une association avec la cellulose, tandis que les deux autres domaines permettent d’y associer une large gamme de molécules chimique ou biologique. Le but est de pouvoir fonctionnaliser la cellulose pour la valoriser. C’est l’ensemble de ces approches de design de protéines mutlidomaines que nous présentons ici.
Dans l’optique d’une neutralité carbone à l’horizon 2050, la valorisation de la biomasse végétale comme source de carbone renouvelable pour la production d’énergie, de matériaux bio-sourcés ou de molécules chimiques fait partie de l’équation. Les microorganismes lignocellulolytiques ont développés tout un arsenal d’enzymes leur permettant de déconstruire la biomasse végétale et de métaboliser le carbone contenu dans les polysaccharides des parois cellulaires. Ces enzymes sont souvent multidomaines et interagissent in vivo avec des substrats insolubles complexes enchevêtrés les uns aux autres. Alors que les domaines de ces enzymes sont en général bien caractérisés in vitro sur des substrats synthétiques solubles, ils le sont rarement dans leur environnement naturel, dense et complexe. Il semble donc pertinent d’interroger l’activité de ces enzymes multidomaines dans leur globalité tout en prenant en compte la conformation et la géométrie spatiale que ces différents domaines peuvent adopter au cours de la catalyse et comment celles-ci influent sur les produits de la catalyse. Mais cette multimodularité peut aussi être mise à profit pour valoriser certaine fraction de la paroi, comme la cellulose. Ainsi, ce polymère abondant est déjà utilisé dans de nombreux secteurs industriels. Faciliter et étendre la possibilité de fonctionnaliser ce biomatériau permettraient d’accroitre ses applications.
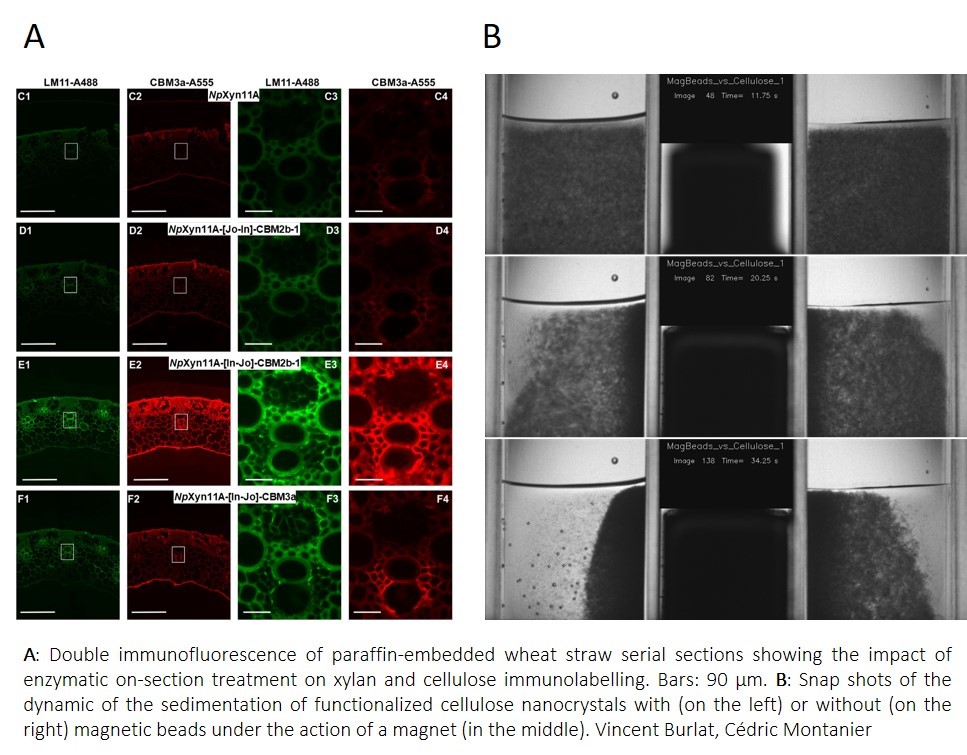
Jo et In sont deux protéines qui s’associent de manière covalente et spontanée. L’asymétrie de cette association ainsi que leur position dans une protéine multidomaine nous a permis de contrôler la géométrie spatiale entre deux domaines; une enzyme dégradant un polysaccharide de la paroi végétale et un domaine de reconnaissance de sucres (CBM). Nous avons résolue les modèles de ces protéines par Small angle X-ray scattering (SAXS) afin d’avoir une image en solution de la position et de la distance entre les deux domaines. Puis nous avons étudié l’activité biologique des différents domaines sur des substrats simples et solubles, jusqu’à des substrats naturels et insolubles, comme la paille ou le son de blé. Les résultats montrent que nos enzymes multidomaines présentent bien une géométrie spatiale dépendante de la manière dont les domaines sont assemblés. La rigidité de l’ensemble due au complexe Jo-In empêche toute interférence physique entre les domaines. De plus, en fonction de la position de Jo et de In, on peut jouer sur l’angle de torsion formé entre les deux domaines. Nous avons montré que cette différence de topologie entre enzyme et CBM avait un impact sur l’activité enzymatique dans des parois de cellules végétales.
Nous avons également développé une plateforme mutlidomaine centrée sur une protéine présentant une forte affinité pour la cellulose. De part et d’autre de cette protéine, nous avons fusionné de manière plus classique deux autres domaines protéiques; l’un permet d’associer des molécules ou des protéines biotynilées, l’autre d’associer par click chimie à l’aide de l’incorporation d’un acide aminé non naturel dans la séquence protéique des molécules chimiques. Il est ainsi possible d’apporter à la cellulose au moins deux fonctions d’intérêt. La modélisation moléculaire de notre protéine chimérique nous a permis d’appréhender la flexibilité de notre modèle et de valider son utilisation. Ainsi, à l’aide d’une seule protéine multidomaine, nous avons marqué par fluorescence des nanocristaux de cellulose que nous avons immobilisé sur des billes paramagnétiques pour les isoler.
Références bibliographiques :
- Bonnet, J. Cartannaz, G. Tourcier, C. Contreras-Martel, J. P. Kleman, C. Morlot, T. Vernet and A. M. Di Guilmi, Sci. Rep., 2017, 7, 43564.
- Enjalbert, M. De La Mare, P. Roblin, L. Badruna, T. Vernet, C. Dumon and C. Y. Montanier, Int. J. Mol. Sci., 2020, 21, 4360.
- Y. Montanier, M. Fanuel, H. Rogniaux, D. Ropartz, A.-M. Di Guilmi and A. Bouchoux, Sci. Rep., 2019, 9, 5763.
Contact : cedric.montanier@insa-toulouse.fr